20MINUTOS.ES
- La Agencia Española de Medicamentos y Productos Sanitarios (AMPS) ha detectado un probable cancerígeno.
- Pide a las personas que lo estén tomando que no interrumpan el tratamiento sin consultar a su médico.
- ¿Qué es la ranitidina? ¿Qué efectos adversos y alternativas tiene?.
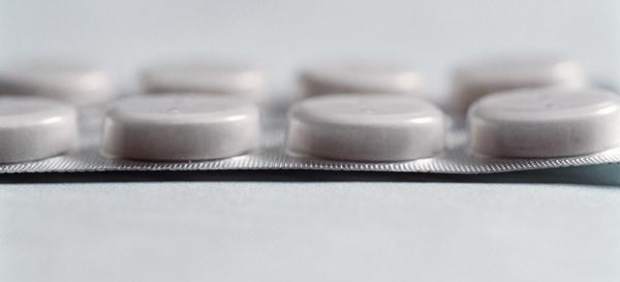
Sanidad ha ordenado con fecha 1 de octubre la retirada preventiva de 16 medicamentos con raditina disponibles en el mercado, una directriz que solo hace referencia de momento a a los comprimidos orales y no a los medicamentos de administración intravenosa por ser esenciales en algunas indicaciones terapéuticas.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ya había informado el 13 de septiembre de que iba a proceder a revisar los medicamentos orales con ranitidina, por la detección de nitrosaminas (N-Nitrosodimetilamina o NDMA), que está clasificado como posible carcinógeno tras estudios en animales. La NDMA está presente en algunos alimentos y fuentes de agua, pero no es probable que cause ningún daño cuando se ingiere en cantidades muy pequeñas.
El ministerio destaca que «no hay evidencia de que la presencia de esta sustancia haya podido producir daño alguno a los pacientes que han consumido el medicamento» y pide a aquellas personas que estén tomando ranitidina que no interrumpan los tratamientos sin consultar a su médico.
Reducir la producción de ácido en el estómago
La ranitidina se emplea para reducir la producción de ácido en el estómago, sobre todo en pacientes con úlcera gástrica o con reflujo gastroesofágico. La AEMPS recuerda que existen alternativas farmacológicas como la famotidina, el omeprazol, pantoprazol o el lansoprazol.
Hay dieciséis comercializadoras afectadas, como Kern Pharma, Ratiopharm España, Normon o Cinfa. Además de por el nombre de ranitidina, también se la puede conocer por los nombres comerciales Zantac, Terposen, Ardoral y Alquen.